La capilaridad de los líquidos |
La capilaridad es una propiedad de los líquidos que depende de su tensión superficial (la cual, a su vez, depende de la cohesión o fuerza intermolecular del líquido), que le confiere la capacidad de subir o bajar por un tubo capilar .
Para entenderlo, veamos un experimento clásico:
En un recipiente se vierte agua (coloreada de un cierto tinte para ver con mayor claridad el efecto que se produce).
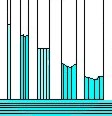
|
| Entre más delgado el capilar, más sube la columna de líquido. |
Se introduce en el recipiente un tuvo de cristal alargado y estrecho. Inmediatamente parte de agua del recipiente ascenderá por el tubo hasta alcanzar una altura determinada, esta altura será tal que el peso del líquido que quede dentro del tubo sea igual a la tensión superficial de dicho líquido.
Si cogemos un tubo con un mayor diámetro el agua que ascenderá por él llegará a menor altura pero el peso del líquido que queda dentro del tubo también es igual a la tensión superficial de dicho líquido.
Si se tuviese un tubo tan fino como el de un cabello, la cantidad de líquido ascendería mucho más en altura pero el peso del líquido que queda dentro del tubo también es igual a la tensión superficial de dicho líquido.
A este fenómeno se le conoce como Capilaridad líquida .
|
|
| Efectos de capilaridad. |
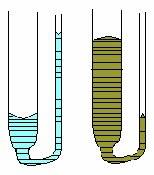
Si tomamos un tubo de cristal grueso comunicado con uno fino y echamos agua en él se verá cómo en el tubo grueso el agua alcanza menos altura que en el fino, como se ilustrra en la figura a la izquierda.
Si hacemos la misma prueba con mercurio en vez de con agua (tal como se compara en la misma figura) resultará que en el tubo grueso el mercurio alcanza más altura que en el fino.
Además, en el primer caso, se puede ver que el agua se une con la pared del tubo (menisco) de forma cóncava , mientras que con el mercurio lo hace de forma convexa .
Cuando un líquido sube por un tubo capilar, es debido a que la fuerza intermolecular (o cohesión intermolecular) entre sus moléculas es menor a la adhesión del líquido con el material del tubo (es decir, es un líquido que moja ).
En palabras más sencillas, cuando se introduce un capilar en un recipiente con agua, ésta asciende por el capilar como si trepase agarrándose por las paredes, hasta alcanzar un nivel superior al del recipiente.
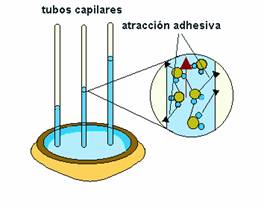
|
| La atracción adhesiva hacia el vidrio es mayor que la adhesión intermolecular del agua. |
El líquido sube hasta que la tensión superficial es equilibrada por el peso del líquido que llena el tubo. Éste es el caso del
agua
, y ésta propiedad es la que regula parcialmente su ascenso dentro de las
plantas
, sin gastar energía para vencer la gravedad.
Sin embargo, cuando la cohesión entre las moléculas de un líquido es más potente que la adhesión a las paredes del capilar (como el caso del
mercurio
), la tensión superficial hace que el líquido llegue a un nivel inferior, y su superficie es convexa.
Ver: Hidrostática
Ver: Presión atmosférica
Fuentes Internet:
http://es.wikipedia.org/wiki/Capilaridad
http://personal.redestb.es/jesusrom/pompas/pompas2.html
http://fernandogonzalezescobar.blogspot.com/2010/06/tension-superficial.html


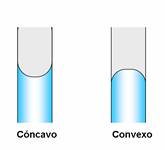 Agua Mercurio
Agua Mercurio