Amadeo Avogadro |

|
| Ampliar imagen |
Amadeo Avogadro (1776-1856). Físico italiano. Interpretó el descubrimiento de Gay-Lussac de que todos los gases se expanden lo mismo al sufrir el mismo aumento de temperatura, como que volúmenes iguales de gases, bajo las mismas condiciones de presión y temperatura, debían estar formados por el mismo número de partículas. Cada partícula, que actualmente recibe el nombre de molécula, puede estar formada por uno o más átomos. En muchos gases, las partículas primarias son moléculas formadas por varios átomos unidos entre sí.
Este descubrimiento permite determinar el peso de diversos átomos o moléculas, relativos al peso de un átomo de hidrógeno, que es el más ligero.
Por ejemplo, si tenemos dos volúmenes iguales, uno de hidrógeno y otro de oxígeno, bajo las mismas condiciones de temperatura y presión, de acuerdo con Avogadro tendrán el mismo número de moléculas. Si ponemos esos gases en dos pequeños tanques iguales, que inicialmente estaban al vacío (comprimiéndolos); el aumento de peso del tanque con oxígeno entre el aumento de peso del tanque con hidrógeno, nos dará el peso molecular del oxígeno en unidades del peso molecular del hidrógeno. El resultado obtenido es 16, o sea que la molécula de oxígeno pesa dieciséis veces más que la de hidrógeno.
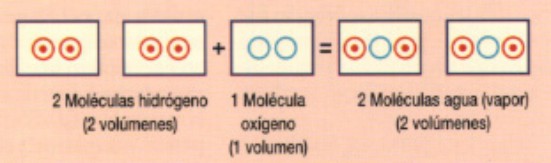
| Esquema de la formación del agua, ampliar imagen |
Como las moléculas de hidrógeno y oxígeno están formadas por dos átomos, el átomo de oxígeno también pesará dieciséis veces más que el de hidrógeno.
El agua, de acuerdo con los descubrimientos de Gay-Lussac , se forma al combinar dos volúmenes de hidrógeno con uno de oxígeno; de acuerdo con Avogadro, su molécula estará formada por dos átomos de hidrógeno y uno de oxígeno (2H + O) y su peso molecular será de dieciocho veces la del átomo de hidrógeno, dos que corresponden al hidrógeno y dieciséis al oxígeno.
Fuente: Páginas Internet