PSU: Química |
Pregunta 12_2005 (química)
Considerando el valor del producto iónico del agua (K W = 1 • 10 –14 ) , la concentración de H + en una solución acuosa 0,1 molar de OH – es
A) 1 • 10
–14
molar
B) 1 • 10
–13
molar
C) 1 • 10
–1
molar
D) 1 molar
E) 13 molar
Contenido: Disoluciones químicas .
Eje temático: Ionización del agua ; Concepto de acidez y el pH .
Clave: B
Curso : Segundo Medio.
Habilidad intelectual medida: Aplicación.
Comentario:
Uno de los aspectos importantes en la química son las reacciones ácido-base , en las que el agua juega un papel preponderante. El agua se disocia parcialmente según la ecuación
![]()
lo cual se describe mediante la constante de equilibrio o producto iónico del agua
![]()
El reducido valor de esta constante significa que el agua está escasamente disociada permaneciendo fundamentalmente en su medio en la forma molecular H 2 O. Sin embargo, cuando se disuelven en agua un ácido o una base se modifican las concentraciones de los iones H + y OH – , sin que se altere la constante de equilibrio, siempre que se mantenga la temperatura constante.
Si la solución acuosa es 0,1 molar en iones OH – la concentración de iones hidrógeno es
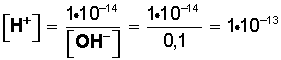
Es importante no olvidar que 10 –14 ( notación científica ) es lo mismo que 0,00000000000001 que se divide por 0,1
por lo tanto la alternativa correcta es la B) .
(Ver: Ionización del agua )
Comportamiento porcentual
Sólo el 45,8 del total de postulantes respondió a la pregunta, y en ese total sólo lo hizo correctamente el 24,7 por ciento.
Nuevamente la omisión es muy alta (54,2 por ciento), lo cual significa que se trató de una pregunta muy difícil, siendo abordada correctamente apenas casi por un cuarto de los estudiantes. La omisión y las respuestas incorrectas pueden atribuirse a dos factores.
El primero se refiere a que se pregunta por concentración de iones hidrógeno en una solución que aparentemente tiene sólo iones OH – y se desconoce la vinculación con el producto iónico del agua.
Un segundo aspecto es el escaso manejo de potencias de 10 , herramienta fundamental en la química básica, especialmente en el comportamiento de ácidos y bases y su relación con el pH.
Fuente Internet:
Publicación oficial del Demre en www.demre.cl

